Mit mér a PCR az allergén analitikában
Az élelmiszerallergén tesztek, a PCR, és különösen a qPCR, egy kiválasztott DNS-szakaszt amplifikál, majd a qPCR esetén fluoreszcens jel alapján követi az amplifikációt és CT, küszöbciklus, értéket ad; a dPCR pedig nagy számú partícióban 0/1, pozitív/negatív, eseményekből számolja vissza a kópiaszámot, így abszolút kvantifikációt is lehetővé tesz standardgörbe nélkül. [13]
A kritikus korlát: a PCR nem az allergén fehérjét/epitópot méri, hanem a forrás-összetevő, faj/anyag, DNS-markerét; ezért a jelenlétet jellemzően közvetett bizonyítékként kell kezelni. [14]
Miért népszerű mégis
A DNS sok esetben hőstabilabb, mint a fehérjék, a PCR pedig alkalmas közeli rokon fajok elkülönítésére, és a szekvenálás/NGS irányába nyit untargeted megközelítést is. [15]
Tipikus teljesítmény: érzékenység, specificitás, LOD/LOQ
Az élelmiszerallergén tesztek PCR-tesztek teljesítménye erősen célpont- és mátrixfüggő, de ipari szempontból a kérdés mindig: milyen alacsony szinten és mekkora bizonyossággal mutat ki, LOD, illetve milyen pontossággal számszerűsít, LOQ. [16]
Konkrét, publikált/összegzett példák:
- A brit hatósági áttekintés említ kereskedelmi zeller PCR megoldást, ahol LOD ~0,4 mg/kg, zellerpor kukoricalisztben, LOQ ~1,0 mg/kg ugyanabban a mátrixban; ugyanitt hangsúlyozzák, hogy más mátrixokra a felhasználónak kell alkalmasságot igazolnia. [17]
- Egy több-laboros vizsgálatban a többfaj-AllNut multiplex qPCR célpontválasztással LOD 0,64 mg/kg, 0,64 ppm, értéket közöl a vizsgált diófélékre vonatkozóan, és kiemeli, hogy a multicopy célpontok javítják a kimutatási képességet. [18]
- dPCR esetén módszertani összefoglalók szerint előny a standardgörbe nélküli abszolút kvantifikáció és a PCR inhibitorokkal szembeni nagyobb tolerancia, ugyanakkor a költség és az áteresztőképesség gyakran rosszabb, mint qPCR-nél. [19]
Nem triviális korlátok: tojás, tej, fajazonos csapdák
A PCR egyes allergéneknél/összetevőknél strukturális okból gyengébb: tojás és tej esetén a DNS-jel gyakran alacsony, és/vagy nem különíthető el a nem allergén szövetektől, ezért módszerválasztáskor ezt előre kezelni kell. [20]
Ipari útmutatók explicit példát adnak: PCR-rel nem lehet megbízhatóan megkülönböztetni, hogy a kimutatott szarvasmarha DNS tej eredetű allergén vagy marhahús eredetű nem allergén komponens; analóg módon csirke/tojás eset. Ez nem apróbetű: rossz döntéshez, rossz címkéhez és rossz visszahívási kockázatkezeléshez vezethet. [21]
Élelmiszerallergén tesztek, PCR munkafolyamat, mintatípusok és validálás
Mintatípusok, amelyekkel a gyakorlatban számolni kell
A professzionális allergén-monitoring tipikusan nem csak késztermék: gyakori a beérkező alapanyag, félkész, késztermék, illetve felületi törlet és öblítő-/mosóvíz vizsgálata. A gyártói útmutatók szerint LFD-k különösen alkalmasak felület/öblítővíz gyors ellenőrzésre, míg ELISA, kvantitatív, és PCR/LC–MS inkább akkreditált labor környezetet igényel. [22]
PCR lépések és a valódi szűk keresztmetszet
A élelmiszerallergén tesztek PCR eredményét általában nem maga a PCR csőben futó része dönti el, hanem a pre-PCR lépések: homogenizálás/őrlés, reprezentatív rész-mintavétel, DNS extrakció, DNS minőség/puritás, inhibitorok kezelése. A gyakorlati leírások tipikus, reprezentatív tesztporció méretként ~100 mg–néhány száz mg finom por frakciót említenek; a DNS extrakciónak jó hozamot, alacsony fragmentációt és inhibitor-mentességet kell adnia. [19]
A PCR ciklusprogram nagyságrendileg órás skálán mozog: tipikusan 5–10 perc kezdeti denaturáció + 35–45 ciklus, denaturáció/annealing/elongáció, + záró elongáció; ez önmagában is ~1–2+ óra lehet, és erre jön rá az extrakció és előkészítés. [23]
Inhibitorok és mátrix-hatások: miért kell módszer + mátrix párosban gondolkodni
A PCR gátlói tipikusan polifenolok, poliszacharidok, sók, zsírok, fűszerekből származó komponensek; ezért a gyakorlatban gyakori trükkök a PVP hozzáadása, polifenolok ellen, nemionos detergensek, zsírtalanítás, alfa-amiláz kezelés keményítős mátrixokra, extra DNS tisztítás vagy hígítás, ha a DNS mennyiség megengedi. [15]
Hatósági áttekintés konkrét példát ad a valós kockázatra: alacsony pH-jú, ecetes/paradicsomos mátrixban a DNS degradálódhat, ami PCR-rel fals negatív eredményt okozhat; ilyen helyzetben ELISA vagy MS előnyösebb lehet. [24]
Kontamináció-kontroll és laborfelépítés
Az élelmiszerallergén tesztek PCR-nél a carry-over kontamináció kezelése nem opcionális. Ipari útmutató explicit minimumként írja le, hogy a PCR-t használó laborban célszerű legalább négy elkülönített terület, ideálisan szoba, a mintapreparálásra, PCR mix készítésre, PCR futtatásra és poszt-PCR műveletekre. [25]
Validálás és minőségbiztosítás
A módszerválasztás egyik legfontosabb, és a gyakorlatban leggyakrabban elszabotált, kérdése: validálták-e az adott tesztet az adott mátrixokra. Az élelmiszerallergén tesztek ipari allergénmenedzsment útmutató ezt konkrét ellenőrzési pontként kezeli, és a labor kiválasztásakor/teszt alkalmazásakor elvárja a mátrix-specifikus validálást. [26]
A validálás nyelve a gyakorlatban standard fogalmakon fut, LOD/LOQ/ismételhetőség/reprodukálhatóság. Például az AOAC teljesítménykövetelmények esetében, ELISA/LC–MS, konkrét küszöbértékek szerepelnek LOD/LOQ és RSD paraméterekre, és ezek jó benchmarkként használhatók a saját követelményrendszer kialakításához. [27]
Egy gyakorlati, CEN-alapú PCR standard struktúrája, például prEN 15634-8 előnézet, külön is jelzi, hogy a workflow része a kontrollok, pozitív/negatív, extrakciós blankok stb., és accept/reject kritériumok definiálása, továbbá a validálás, specificitás, szenzitivitás, ring trial. [28]
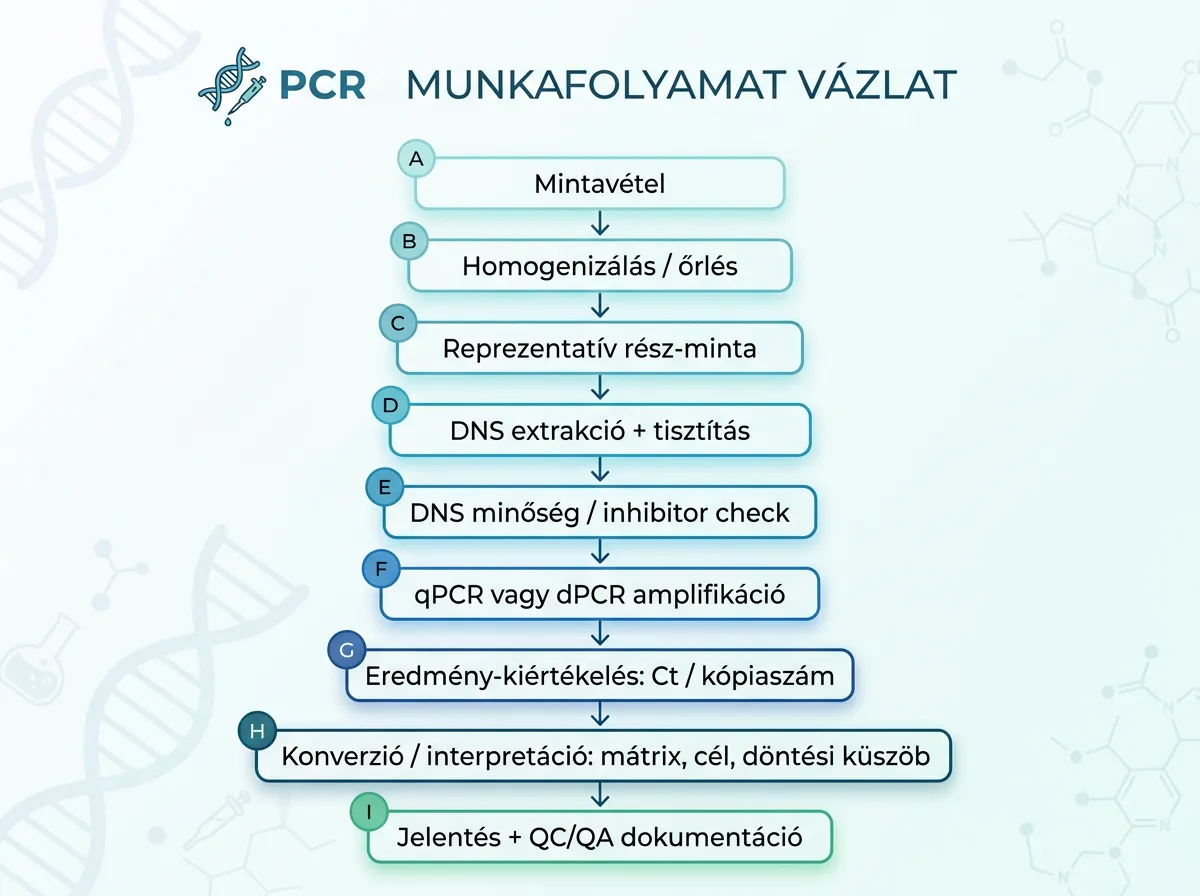
A fenti lépéssor a nemzetközi gyakorlatban is kivonatolható így: pre-PCR lépések dominálnak a hibakockázatban; a dPCR/qPCR különbség a kvantifikáció módjában és inhibitor-tűrésben jelenik meg. [15]
Szabványok és szabályozási keret
Miért kell a szabályozást érteni, ha csak mérést végzel
Az EU-ban a kötelező allergénjelölés alapja a 1169/2011 rendelet, amely az Annex II listában sorolja a jelölendő allergéneket. Ez közvetlenül meghatározza, mely allergénforrásokra kell a gyártónak és a laboratóriumnak kontrollrendszert építenie. [29]
Az USA-ban a főallergének jelölési rendszere, FDA, dinamikusan változott az utóbbi években: a FASTER Act alapján a szezám 2023. január 1-től kötelezően jelölendő major allergen az FDA által szabályozott csomagolt élelmiszereken. Nem EU-s exportnál ez nem érdekesség, hanem megfelelőségi kockázat. [30]
PAL és a mennyit kell tudni kérdése
Ipari útmutatók szerint az EU-ban a szándékolatlan allergénjelenlétre vonatkozó precautionary allergen labelling, PAL, jelenleg nem egységes, explicit jogszabályi rendszerben mozog, ezért a vállalatok és hatóságok gyakorlata országonként eltérhet; ez a mérési stratégiát is befolyásolja az élelmiszerallergén tesztek során, pl. milyen action level alá kell látni. [31]
A kockázatalapú küszöbök, reference dose logika, ipari környezetben megjelennek: az AOAC SMPR például arra vezet le példát, hogy a referencia dózis és adagméret alapján hogyan állítható be kvantifikációs cél, pl. mg protein/100 g. [32]
Akkreditáció és labor-szintű megfelelés
A laborok kompetenciájának és konzisztens működésének alapnyelve az ISO/IEC 17025, amely a kompetencia, pártatlanság és következetes működés követelményeit fogalmazza meg; ez az élelmiszerallergén tesztek tesztek validálása, mérési bizonytalansága és jelentésminősége szempontjából közvetlenül releváns. [33]
Módszer-szabványok: CEN horizontális keretek
Az európai szabványosítás élelmiszerallergén tesztek analitikában horizontális módon épül:
- EN 15842: általános megfontolások és validálási elvek az immunoassay, nukleinsav-alapú és LC–MS típusú módszerek kapcsolatáról. [34]
- EN 15633-1: immunológiai módszerek, antitest-alapú, általános kerete. [35]
- EN 15634-1: molekuláris-biológiai, PCR, módszerek általános kerete allergénforrást hordozó fajok DNS-szekvenciáira. [36]
- EN 17644: LC–MS módszerek általános megfontolásai allergének peptid/protein szintű kimutatására. [37]
Alternatív módszerek és összehasonlítás
Módszercsaládok: mikor helyes és mikor hibás választás
Az ipari útmutatók és hatósági áttekintések egy irányba mutatnak: nincs univerzális módszer, amely minden allergént, minden mátrixban, minden feldolgozottsági szinten hibamentesen kezel az élelmiszerallergén tesztek során. A módszert a kérdés, screening vs megerősítés vs kvantifikáció, a mátrix, zsíros, savas, polifenolos, erősen hőkezelt, és az allergénforrás alapján kell kiválasztani. [38]
Az ELISA előnye, hogy fehérjét mér, és sok esetben kvantitatív; viszont a feldolgozás befolyásolhatja az immunreaktivitást és a különböző kitek eltérő standardokat/egységeket használhatnak, ami összehasonlíthatósági problémát okoz. [39]
A laterális flow/LFD tipikusan jó üzemi döntéstámogató, line-clearance, CIP utáni gyors check, de nem alkalmas finom kvantifikációra. [3]
A célzott LC–MS/MS akkor indokolt, amikor több allergént kell egyszerre megbízhatóan vizsgálni, vagy amikor ELISA/PCR konfliktusos eredményt ad, és bíróságállóbb megerősítés kell; ugyanakkor drága és időigényes. [40]
A DNS-barcoding / metabarcoding / NGS inkább faj- és összetevő-azonosítási probléma, összetevő-felderítés, autentikáció, többfaj-mix, és kevésbé klasszikus trace allergén kvantifikáció, de a rejtett allergénforrás azonosításában erős lehet. Egy 2025-ös, növényi allergénforrásokra fókuszáló DNS-barcoding vizsgálat ITS2 jelölővel ~98% feletti azonosítási pontosságot jelentett kereskedelmi élelmiszerekben, miközben sok minta nem tartalmazott allergénjelölést. [41]
Összehasonlító táblázat az allergén teszttípusokról
| Szempont | qPCR, valós idejű PCR | dPCR, ddPCR/cdPCR | ELISA, mikrotiter | LFD/LFIA, laterális flow | LC–MS/MS, célzott proteomika | DNS barcoding / metabarcoding / NGS | Multiplex immunoassay / bioszenzor rendszerek |
|---|---|---|---|---|---|---|---|
| Tesztkategória | qPCR, valós idejű PCR | dPCR, ddPCR/cdPCR | ELISA, mikrotiter | LFD/LFIA, laterális flow | LC–MS/MS, célzott proteomika | DNS barcoding / metabarcoding / NGS | Multiplex immunoassay / bioszenzor rendszerek |
| Elv | DNS amplifikáció, fluoreszcens detektálás, Ct alapú kvantifikáció | partícionált PCR, abszolút kópiaszám | antitest-alapú fehérje/epitóp marker detektálás | immunkromatográfia, vizuális csík | fehérje emésztés → peptid marker → MS/MS kvantifikáció | standard marker + szekvenálás; több faj azonosítása | több célpont egy panelen; mikrofluidika/optika/elektrokémia |
| Tipikus célpont | faj/összetevő DNS-marker | DNS-marker | allergénforrás fehérjei vagy markerei | fehérje marker | allergén-specifikus peptidek | fajazonosító DNS régiók, pl. ITS2 | több allergén fehérje marker / DNS fragment |
| Érzékenység | mg/kg szintig lemehet; példa: zeller PCR LOD ~0,4 mg/kg, LOQ ~1,0 mg/kg adott mátrixban [42] | alacsony kópiaszámnál magasabb precizitás; kevésbé inhibitor-érzékeny; egyes platformoknál jobb érzékenység qPCR-hez képest [48] | alacsony mg/kg szint; AOAC peanut ELISA SMPR: LOD/LOQ ≤10 ppm, mátrixfüggő [49] | tipikusan mg/kg körül; példa: egyes teszteknél ~1 mg/kg DL és ~10 perc eredmény [54] | AOAC SMPR 2016.002: MDL ppm szinten, pl. ≤3 ppm több allergénre, és MQL ≤10 ppm, célpontfüggő [60]; publikált peanut módszer: LOD 0,25–0,5 mg/kg [61] | azonosítási pontosság: ITS2-alapú módszer ~98%+ azonosítás kereskedelmi mintákban [41] | mikrofluidikus ELISA: 15–20 perc teljes assay időt is közöltek gluten és Ara h 1 esetén [67] |
| Specificitás | Jó faj-specifikusság, de közvetett, DNS≠fehérje; egyes esetekben fajazonos csapda, tej vs marhahús [43] | hasonló faj-specifikus logika; közvetett marad, DNS [44] | keresztreakció, pl. zeller/Apiaceae, feldolgozás és extrakció torzíthat [50] | alapvetően ELISA-szerű antitest-korlátok; lot variabilitás lehet [55] | magas analitikai specificitás, peptid, de peptidválasztás és mátrix-szuppresszió kritikus [62] | erős fajazonosítás, de kvantifikáció és trace érzékenység korlátozott/komplex | függ a receptoroktól, antitest/aptamer; mátrixhatás továbbra is tényező |
| Minta-előkészítés | homogenizálás + DNS extrakció + inhibitor kezelés [44] | mint qPCR + plusz partícionálás [44] | fehérje extrakció, kritikus buffer/mátrix [51] | egyszerű extrakció / swab [56] | emésztés + cleanup; időigényes [63] | DNS extrakció + könyvtárkészítés + bioinformatika | változó; gyakran speciális cartridge/platform |
| Idő az eredményig | analízis tipikusan 2–3 óra; lab turnaround gyakran 1–3 nap [45] | hosszabb hands-on; throughput alacsonyabb; költség/szám magasabb lehet [44] | analízis 2–3 óra; turnaround gyakran 1–3 nap [43] | percek, tipikusan ~10 perc [57] | analízis 2–3 óra; turnaround akár ~5 nap; prep akár ~2 nap [64] | tipikusan ≥1 nap, workflow-függő | percek–órák |
| Költségszint | közepes | közepes–magas | alacsony–közepes | alacsony | magas | közepes–magas | közepes–magas |
| Szabványos/elfogadottság | CEN horizontális keretek, EN 15634-1, EN 15842 [46] | ipari standardizáció még kevésbé érett; jó kiegészítő metrológiai irány [44] | CEN immunoassay keret, EN 15633-1, EN 15842; AOAC SMPR-ek [52] | széles ipari használat verifikációra; validálásra korlátozott [58] | CEN LC–MS keret, EN 17644, AOAC SMPR 2016.002 [65] | inkább autentikációs standardizáció; allergén screeningre feltörekvő [66] | gyorsan fejlődő, de heterogén; validálási teher magas |
| Legjobb felhasználás | feldolgozott mintákban fajjelenlét; ELISA hiányában vagy konfliktusban megerősítés [47] | abszolút kvantifikációs igény; alacsony szintű célpontok; qPCR validáció támogatása [44] | kvantitatív gyártási kontroll, cleaning validation, hivatalos minta [53] | üzemközi gyors ellenőrzés, felület, öblítővíz, line-clearance [59] | megerősítő vizsgálat, multi-allergen screening, vitás esetek [64] | összetevő-felderítés, rejtett/nem deklarált fajok azonosítása [41] | on-site kvantifikációs proof-of-concept; gyors screening különleges igényekre [68] |
Ajánlások és további olvasmányok
Ajánlások gyakorló szakembereknek
A módszerválasztást érdemes kíméletlenül egyszerű logikára visszanyomni: mit akarsz bizonyítani, milyen döntést hozol belőle, és mennyibe kerül egy rossz döntés, visszahívás, hamis biztonságérzet, fölösleges PAL, vitás hatósági ügy. Az alábbi keretrendszer a legstabilabb ipari/hatósági tanulságokra épül:
- Ha üzemközi gyors döntés kell, takarítás után, átálláskor: LFD/LFIA. De tartsd fejben: validálásra nem ez a fő eszköz, és rendszeres ELISA-val való összevetés kell. [69]
- Ha kvantitatív kontroll kell, cleaning validation, termék felszabadítás, hatósági kockázat: ELISA első vonal, különösen ha a cél a fehérje-markerek mérése és van megfelelő kit. Az AOAC-szerű teljesítménykritériumokat, LOD/LOQ/RSD, használd belső minimumként. [70]
- Ha ELISA nincs / kétes / keresztreakciós kockázat magas, vagy növényi allergénforrás DNS-e stabil: PCR lehet másodlagos megerősítés vagy fő módszer. De csak akkor, ha a célpont/mátrix páros validált, és érted a DNS≠fehérje korlátot, tej/marhahús; tojás/csirke. [71]
- Ha konfliktusfeloldás, multi-allergen megerősítés, vagy közel-hazard mérés kell: LC–MS/MS. Számolj magas költséggel és hosszabb átfutással; és fogadd el, hogy a mintapreparálás lesz a fő idő/kockázat. [4]
- Ha az igazi kérdés rejtett összetevő/fajazonosítás, autentikáció + allergénforrás-felderítés: DNS barcoding / NGS irány. Nem elsődleges trace kvantifikáció, de nagyon hasznos lehet, amikor a beszállítói vagy összetevő-információ hiányos vagy gyanús. [66]
Ami nem tárgyalható kompromisszum: módszer- és mátrix-validálás, és a referenciaanyagok/QC anyagok hiányának tudatos kezelése. Hatósági áttekintések szerint éppen a referenciaanyagok hiánya és a teljes körű, mátrix-széles validálás hiánya a legnagyobb evidence gap. [72]
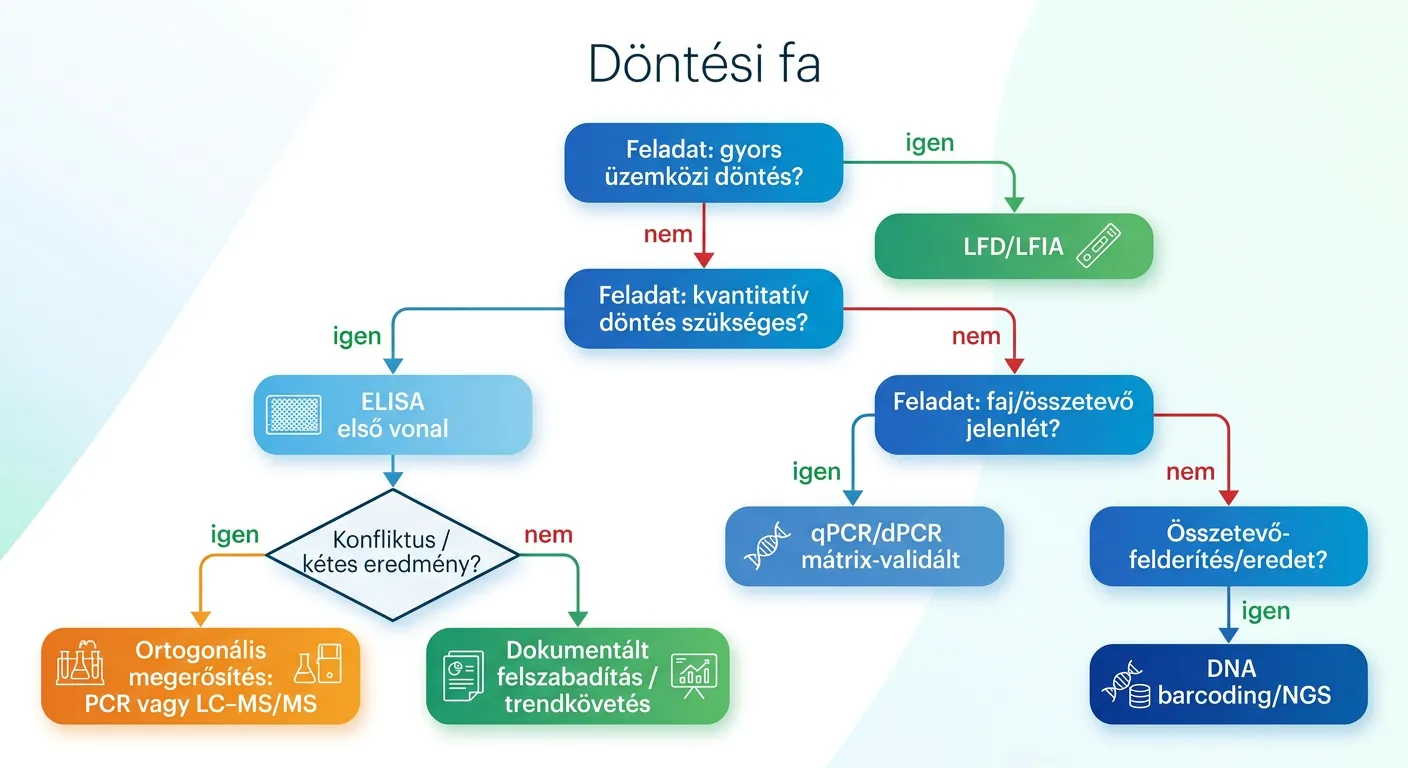
A fenti döntési fa nem tankönyvi: pont azokat a tipikus hibákat próbálja kizárni, amelyeket a hatósági és ipari összefoglalók visszatérően említenek, mátrixfüggő fals negatív PCR; ELISA keresztreakció; túlzott bizalom gyorstesztben; referenciaanyag hiánya. [10]
Az általunk forgalmazott élelmiszerallergén tesztek »
Javasolt további olvasmányok és primer források
- Wageningen Food Safety Research 2024.007
- FoodDrinkEurope 2022 – Guidance on Food Allergen Management for Food Manufacturers
- Google Search Central – Creating helpful, reliable, people-first content
- Google Search Essentials
- UK Food Standards Agency – Evidence gaps in allergen management and testing
- Google – E-E-A-T and quality raters guidance
- Google – Article structured data
- Google – FAQ and HowTo changes
- UK Food Standards Agency – Allergen detection methods unbiased literature search
- Springer – AllNut multiplex qPCR study
- AOAC SMPR 2018.012 – Peanut ELISA
- prEN 15634-8 preview
- EU 1169/2011 rendelet
- FDA – FASTER Act and sesame allergen
- ISO/IEC 17025:2017
- EN 15842
- EN 15633-1
- EN 15634-1
- EN 17644
- ScienceDirect – Plant allergen source DNA barcoding study
- R-Biopharm lateral flow example
- AOAC SMPR 2016.002 – LC–MS allergen methods
- ScienceDirect – Peanut LC–MS method
- PMC – LC–MS allergen analytics review
- PMC – Multiplex immunoassay / biosensor systems